Что делать, если ржавеет нержавейка. Контактная коррозия металлов: причины возникновения, способы защиты
Может ли нержавейка ржаветь?
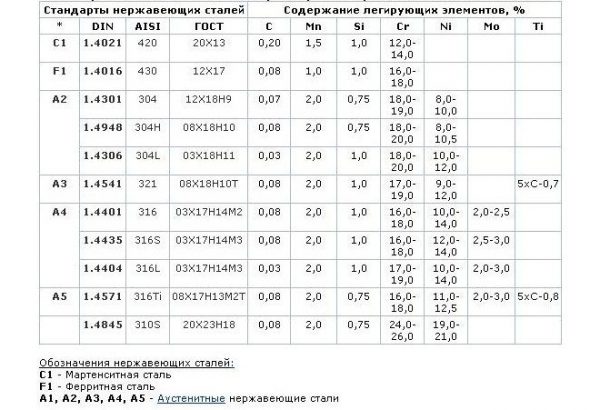
Существует три группы нержавеющих сталей, каждая из которых имеет свои особенности и специфику применения:
- Коррозионностойкая сталь. Имеет высокую стойкость к коррозии в неосложненных условиях – в быту, на производстве.
- Жаростойкая сталь. Обладает термостойкостью, не ржавеет при повышенных температурах, может применяться на химических заводах.
- Жаропрочная сталь. Остается механически прочной при высоких температурах.

Таким образом, не все виды нержавейки предназначены для эксплуатации в той или иной агрессивной среде. К примеру, использование обычной нержавеющей стали на пищевом производстве, частое мытье с хлорсодержащими средствами вызовет быструю порчу материала. Аналогично применение металла в морской воде приведет к повышению скорости коррозии в разы.
Также ржавчина часто появляется на нержавейке после сварки (термической обработки), которая была произведена без соблюдения определенных правил. После механического повреждения металла последствия будут аналогичными: в месте дефекта возникнет точечная коррозия. Гладкий, полированный материал обычно ржавеет менее интенсивно, чем шероховатый: на последнем элементы коррозии могут появиться гораздо быстрее.
Защита от ржавчины нарушается там, куда попала раскаленная окалина, поскольку от сильного повышения температуры в нежаростойкой стали происходит выгорание легирующих веществ (в основном хрома). После прогорания дыр их края и прилегающие зоны становятся подверженными коррозии, хотя более глубокие слои металла чаще всего остаются неповрежденными. Спасти нержавейку поможет обработка травильными пастами, специальными эмульсиями.
Прочие причины коррозии нержавеющей стали:
- контакт материала с обычной углеродистой сталью (в том числе посредством инструментов, которыми раньше резали простую сталь);
- регулярная чистка металлическими щетками;
- игнорирование механической или химической обработки сварного шва.

Причиной коррозии металла может стать и его изначально низкое качество. Стойкость стали к ржавлению обусловлена присутствием хрома в достаточном количестве. Этот элемент после воздействия воды, воздуха, кислот и щелочей формирует тончайший непроницаемый слой, который не дает материалу ржаветь. Если хрома в составе мало либо он распределен неравномерно, создание и поддержание оксидного слоя становится невозможным.
к содержанию ↑
4. Классификация коррозионных процессов по характеру коррозионного разрушения.
4.1 Контактная коррозия.
Контактная коррозия образуется при контакте разных металлов в присутствии электролита или влажного воздуха. В образовавшейся гальванопаре, металл с более электроотрицательным потенциалом становится анодом и разрушается в первую очередь, тогда как более электроположительный металл – катодом.
В качестве примера можно рассмотреть железо (рисунок 4). Цинк, алюминий и кадмий (последний — в солевой среде) являются анодами для стали, а значит именно они будут окисляться в первую очередь, тогда как олово, хром, медь, свинец, никель – катодами, а значит железо будет подвержено глубокой локальной коррозии, пример изображён на рисунке.

Рисунок 4 – Примеры контактной коррозии на стали.
4.2 Щелевая коррозия.
Щелевая коррозия – это коррозия, возникающая в случаи, если часть металла изолирована от основного участка неметаллическим материалом (резиной, деревом, пластиком и т.д.). Пример такой коррозии можно наблюдать в трубах в месте соприкосновения с сальником (рисунок 5). Образование полости под сальником вызывает протечки в трубах. При наличии таких неровностей коррозионная жидкость застаивается в щели, где и происходит бурная коррозия металла.
Причиной щелевой коррозии является пониженная концентрация окислителей в зазорах по сравнению с объёмом раствора и замедленный отвод продуктов коррозии. В результате их накопления меняется pH раствора в щели, что так же ускоряет коррозию.
Металл в щели и металл открытой поверхности образуют макропару:
Me — 2е = Me2+ (внутри щели)
0,5О2 + H2O + 2е = 2ОН- (на поверхности металла)
Поскольку площадь открытой поверхности гораздо больше, чем внутри щели, плотность тока коррозии внутри щели оказывается чрезвычайно высокой.

Рисунок 5 – Кислородная концентрационная ячейка под сальником.
По мере протекания коррозии внутри щели накапливается избыточный положительный заряд. Ионы ОН- устремляются в щель, чтобы нейтрализовать этот заряд. В результате, на внутренней поверхности щели осаждается гидроксид металла, что ещё больше сокращает эффективную площадь анода.
4.3 Питтинговая коррозия.
Питтингом называют глубокие поражения (точечные язвы) на поверхности металла (рисунок 6). Питтинговая коррозия, вследствие своей локализованности и малой заметности, является одним из наиболее опасных видов коррозионного разрушения. Не следует путать питтиговую коррозию с питтингом на никелевых покрытиях.
Так как пассирующий слой на поверхности металла не является гомогенной системой, то коррозия возникает из-за наличия анодных и катодных участков на поверхности. В возникшей гальванопаре анодом является питтинг, а катодом – остальная часть поверхности. На аноде происходит высвобождение электронов, которые восстанавливают кислород на катодной пассивированной части поверхности.

Рисунок 6 – Виды питтингов: а – открытый с защитным слоем на окружающей поверхности; б – закрытый, без окружающего защитного слоя; в – закрытый, с окружающим защитным слоем. 1 – металл; 2 – раствор; 3 – защитный слой; 4 – пористые продукты коррозии; 5 – крышка над питтингом; 6 – отверстия в крышке.
Развитию питтинга способствуют различного рода дефекты на поверхности пассивной плёнки, например, царапины, сколы, поры, посторонние включения. Также для возникновения питтинга необходимо, чтобы в растворе одновременно находились активаторы питтинговой коррозии (Cl-, Br-, J-, CN-) и пассиваторы металла (OH-, SO42-, NO3-,ClO4-).
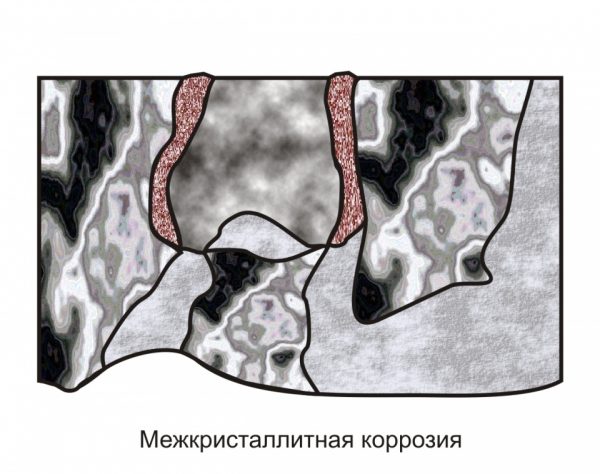
4.4 Межкристаллитная коррозия.
Межкристаллическая коррозия возникает из-за разницы потенциалов на границе зерна и в его матрице (рисунок 7).
На воздухе на границе зерна образуется карбидная фаза, что сдвигает потенциал в область более электроотрицательных значений. Таким образом граница зерна является анодом по отношению к их матрице.
Наиболее опасен данный тип коррозии для сплавов, так как в месте скопления более электроотрицательного металла будет образовываться анод, а основного – катод. Например, для нержавеющих сталей, содержащих хром, вблизи границ зёрен содержание хрома оказывается ниже, чем на остальной поверхности, что делает их менее пассивированными. Вследствие этого такие места становятся анодами по отношению к матрице зерна.

Рисунок 7 – Межкристаллическая коррозия нержавеющей стали: 1 – катод; 2 – анод; 3 – карбидная фаза; 4 – зона, обеднённая хромом; 5 – граница зёрен.
4.5 Фреттинг-коррозия.
Фретинг-коррозия происходит между двумя поверхностями, находящимися в непрерывном контакте друг с другом и совершающими малые колебания. Поверхности никогда не отрываются друг от друга, поэтому в точках механического контакта происходит накопление осколков продуктов коррозии.
Данная коррозия возникает при незначительных колебаниях, циклических или возвратно-поступательных движений с малыми амплитудами и скоростями.
Этой коррозии подвергаются болты, заклёпки, шарниры, муфты, клапаны, детали двигателей и пр.
4.6 Коррозионное растрескивание под напряжением.
Коррозионное растрескивание под напряжением возникает, когда металлическое изделие подвержено растяжению в коррозионной среде. Тогда даже при напряжениях ниже напряжения разрушения происходит растрескивание, в конце концов, приводящее к разрушению конструкции или изделия.
На растянутых участках металла идёт коррозия, поскольку они оказываются анодами по отношению к нерастянутой части. Это явление наблюдается на любых металлах и сплавах, а также в любых средах.
4.7 Коррозионная усталость.
Коррозионная усталость возникает вследствие одновременного воздействия агрессивной среды и механической нагрузки.
Коррозионная усталость часто бывает причиной «неожиданного» разрушения металлических деталей, так, если деталь, находящаяся в коррозионном окружении, подвержена непрерывным вибрациям, её разрушение происходит при напряжении гораздо ниже предела выносливости.
Факторы, определяющие стойкость металла к коррозии
Чтобы металл не был подвержен коррозии, он должен пройти пассивацию – переход поверхности в неактивное (пассивное) состояние, при котором на ней формируется тонкий защитный слой. Хорошая нержавейка быстро и легко пассивируется при обычных атмосферных условиях – контакте с кислородом из воздуха. Чем больше хрома в составе стали, тем выше ее пассивационная способность и антикоррозионные свойства.
Кроме хрома, легирование стали производят с помощью никеля. Он тоже способствует пассивации, но в чуть меньшей степени. Оба металла придают наивысшую антикоррозионную стойкость, хотя в состав стали могут вводиться и иные элементы: медь, ниобий, молибден. Для усиления защитных свойств любые добавки должны находиться в стандартном состоянии, а при изменении их структуры стойкость к коррозии падает (например, при переходе хрома в форму нитрида, карбида). Это может произойти во время контакта с сильными кислотами: серной, соляной, плавиковой.
к содержанию ↑
Пассивный слой
Под пассивным слоем понимают тонкую оксидную пленку, которая формируется на стали после реакции хрома с кислородом. Она благоприятно воздействует лишь на свойства нержавейки: на обычной стали кислород при взаимодействии с атомами железа провоцирует формирование мелких пор и появление ржавчины. Слой коррозии тоже будет называться пассивным, ведь он реакционно инертен по отношению к окружающей среде.
к содержанию ↑
Условия и причины разрушения защитного слоя нержавеющей стали
Нержавейка получает свои улучшенные качества при добавлении легирующих элементов в состав сплава. В основном этими добавками служит хром, никель, молибден. В первую очередь за антикоррозийные свойства отвечает хром, чем больше его в составе, тем лучше формируется антикоррозийный слой на поверхности металла. Атомы хлора вступают в реакцию с кислородом, впоследствии чего образуется оксидная пленка.
Соответственно, больше всего подвержены коррозии те сплавы, в которых меньше легирующих добавок в составе, в частности хрома и никеля.
Внешний слой сплава может портиться от контакта с железом. Это возможно, например, при неправильной сварке, когда на поверхность попадают частички железа. Если после этого плохо провести обработку детали, на сварочном шве появятся коррозионные вкрапления, которые впоследствии будут увеличиваться.
Разрушение защитного слоя на нержавейке и возникновение коррозии обусловлено несколькими факторами:
- Неправильная обработка поверхности металла. При нарушенной технологии сварки или шлифовки детали образуются микродефекты, которые приводят к разрушению оксидной пленки.
- Использование некачественных материалов. Это относится к низкосортной стали, когда экономия денег сказывается на качестве сплава.
- Неправильная эксплуатация.
Во избежание возникновения ржавчины на нержавейке следует тщательно подходить к выбору предприятия, занимающимся изготовлением и продажей нержавейки. Обязательным критерием выбора должен послужить опыт работников и заключение договора с гарантийными условиями.
Если вам поступило предложение купить нержавейку по цене ниже рыночной, то стоит задуматься о качестве материала.
Виды коррозии нержавеющей стали
По типу развития, причине появления и признакам выделяют несколько видов коррозии нержавейки.
Щелевая коррозия нержавеющих сталей
Щелевая коррозия – широко распространенный вид ржавления нержавейки. Она развивается там, где есть небольшой зазор в конструкции, например, когда вода проникает под крепежные элементы внутрь изделия. Второй поверхностью при этом обычно выступает резиновый уплотнитель, прокладка, а порой и металлический элемент.
Механизм формирования щелевой коррозии таков:
- Скопление агрессивных ионов в зазоре, вытеснение кислорода.
- Появление анода в зазоре (материал вне зазора при этом играет роль катода).
- Образование коррозии из-за изменения кислотности среды и электрохимических реакций.

Чтобы предотвратить щелевую коррозию, нужно правильно проектировать конструкции. Важно обеспечивать катодную защиту, которая снизит кислотность, а также улучшать текучесть среды.
к содержанию ↑
Общая поверхностная коррозия
Общей коррозией называют равномерное нарушение структуры металла в части поверхностного слоя. Она вызывает разрушение оксидной пленки на большей части изделия или по всей его площади. Обычно причиной является контакт с сильными щелочами, кислотами, соединениями йода, фтора, брома. Главным же «врагом» нержавейки считается хлор – именно поэтому для ее чистки нельзя применять хлорсодержащие моющие средства.
к содержанию ↑
Точечная коррозия (питтинг)
Больше всего питтинговой коррозии подвержены именно нержавеющие стали, а также сплавы на основе алюминия, никеля. В отличие от обычной стали, которая чаще страдает от общей поверхностной коррозии, такие материалы в большинстве случаев покрываются именно питтингами – мелкими дефектами. Локальное разрушение пассивного слоя происходит в таких ситуациях:
- царапание, механическое повреждение;
- местное изменение состава стали;
- точечное воздействие ионов хлора, серы, галогенидов;
- повышение температуры.

Точечное ржавление считается самым распространенным среди разных видов нержавейки. Из-за него в баках появляются дырки, в трубах, резервуарах – мелкие трещинки. Обычно их диаметр составляет не более 1 мм, при этом глубина может быть значительной – в этом состоит коварство данного явления. Как и в случае со щелевой коррозией, в роли анода будет выступать конкретный питтинг, а катодом станет остальная (неповрежденная) поверхность. Добавление молибдена к нержавеющей стали при ее производстве увеличивает стойкость изделий к точечной коррозии.
к содержанию ↑
Интеркристаллическая коррозия
У такого процесса есть еще одно название – межкристаллитная коррозия нержавеющих сталей (МКК). Она возникает при резком повышении температуры, что случается, например, при сварке. Ржавление начинается, если при участии нагрева вдоль границ зерен проступает карбамид хрома, то есть структура этой легирующей добавки кардинально меняется. Для ферритной стали достаточная температура для формирования очагов коррозии равна +900 градусам, для аустенитной стали – +450 градусам.
к содержанию ↑
Контактная коррозия
Данный вид коррозии развивается при прямом контакте разнородных металлов друг с другом под действием электролитов. К примеру, такое случается при состыковании разных металлических изделий в агрессивной токопроводящей среде – морской воде. В результате сталь локально портится, а менее благородные металлы могут и вовсе раствориться.
Профилактические меры
Не допустить развитие контактной коррозии поможет выполнение некоторых правил. Не стоит использовать без особой необходимости защитные металлические покрытия, особенно если детали будут:
- свариваться внахлест;
- соединяться заклепками из другого металла;
- использоваться в районах с жарким влажным климатом, в прибрежной зоне.
Если верхнее защитное покрытие уже нанесено, перед проведением сварки или клепки его нужно снять в местах будущего соединения. Полимерных покрытий это ограничение не касается.
Между двумя разными металлами допустимо располагать специальные прокладки. Например, при использовании металлоконструкций в морской воде такие прокладки изготавливают из магния, алюминия, цинка, свинца. Изоляцией могут выступать также полимерные материалы, лакокрасочные покрытия.
Основная рекомендация – использование в одной конструкции одинаковых либо сочетающихся друг с другом металлов. Тщательное внимание нужно уделять обработке поверхностей контактирующих деталей – она должна быть идентичной, если иного не требуют конструкционные особенностей изделия. При сваривании нужно корректно выбирать химический состав сварочной проволоки. Это же касается выбора материала заклепок при соединении клепкой.
Вернуться назад
Популярные статьи
В чем отличие отожженной и неотожженной медной трубы?05.07.2022
Еще с прошлого столетия медь закрепила за собой статус одного из самых долговечных материалов, обладающих стойкостью к широкому диапазону температурного воздействия и коррозийным процессам, непроницаемостью для агрессивных веществ. В связи с этим продукция из меди активно применяется в …
Читать далее

Какой провод сильнее нагревается: медный или стальной?05.07.2022
Подача электроэнергии потребителю и ее использование в больших мощностях пока невозможно без проводов и кабелей.
Медь и ее сплавы с самого начала освоения электричества для человечества активно применялись в силу их достоинств: хорошей электро- и теплопроводности, механической прочност…
Читать далее

Акмарал СыргабаеваРуководитель отдела продажПроконсультируйтесь с нами бесплатно
- Поможем выбрать металлопрокат
- Найдем редкий сортамент металлопроката и редкие марки стали
- Рассчитаем стоимость заказа и назовем сроки отгрузки
Ваш телефон*Получить консультациюНажимая кнопку, вы соглашаетесь с условиями обработки персональных данных 
Крупнейший торгово-складской комплекс Казахстана по продаже металлопроката.
Все права защищены. Копирование информации преследуется по закону РК.
© 2010-2022 / ТОО «Казметсервис»
Сайт разработан ROIburo
Продукция
- Листовой прокат
- Трубный прокат
- Сортовой прокат
- Фасонный прокат
- Тросы
- Канаты
- Нержавеющий прокат
- Цветной прокат и сплавы
- Специальные стали
- Трубопроводная арматура
- Оцинкованная сталь
- Фильтры и очистительное оборудование
- Блоки ФБС
- Трубная изоляция
- Пружины
- Изоляционные материалы
- ЖБИ изделия
- Фасадный декор
- Уплотнители
- Пожарное оборудование
- Металлоконструкции
- Фреоны, хладоны, хладагенты
- Инструменты и оборудование
- Производство
Информация
- Новости
- О нас
- Наши сотрудники
- Клиентам
- Спецпредложения
- Контакты
- Услуги
Контакты
[email protected]
+7 (7273) 123-444
Пн — Пт: 09:00 — 18:00
Сб, Вс — выходной
пр. Райымбека 348/4 офис 613 (БЦ Aspara)
Скачать прайс-лист
Оставить отзыв
Оставить отзыв о нашей работе или сотруднике
Оставить отзыв о компании Вы можете, заполнив форму обратной связи. Выберите подходящий вариант.
ПожаловатьсяПоблагодаритьБлагодарность
Чтобы оставить положительный отзыв о работе нашего филиала или сотрудника, пожалуйста, заполните все поля формы ниже
Ваше имяВаш email*Текст сообщения
<текстареа class="form-group__input m-form__текстареа" id="g-text" name="text"> ОтправитьНажимая кнопку отправить, вы соглашаетесь
с правилами обработки персональных данных Спасибо!
Ваша жалоба направлена в отдел по работе с клиентами
Спасибо!
Ваш отзыв направлен в отдел по работе с клиентами
Жалоба
Чтобы оставить жалобу, пожалуйста, заполните все поля формы ниже
Ваш email*Ваш телефон*Текст сообщения
<текстареа class="form-group__input m-form__текстареа" name="text" id="co-text"> ОтправитьНажимая кнопку отправить, вы соглашаетесь
с правилами обработки персональных данных Заказ обратного звонка
Вы всегда можете обратиться к нашим специалистам отдела продаж.
Мы перезвоним вам в течение 15 минут и будем рады помочь!
Ваше имяВаш телефон*ОтправитьНажимая кнопку отправить, вы соглашаетесь
с правилами обработки персональных данных Заявка отправлена
Мы свяжемся с вами в течение 15 минут и проконсультируем по любому вопросу!
НазадСтрана
- Казахстан
- Кыргызстан
- Узбекистан
Ваш город
- Алматы
- Нур-Султан (Астана)
- Атырау
- Актау
- Актобе
- Жезказган
- Караганда
- Кокшетау
- Костанай
- Кызылорда
- Павлодар
- Петропавловск
- Семей
- Талдыкорган
- Тараз
- Туркестан
- Уральск
- Усть-Каменогорск
- Шымкент
Добавлено в заявку Продолжить покупки Перейти в корзину Узнать стоимость:Ваше имяВаш телефон*ОтправитьНажимая кнопку «Отправить», Вы соглашаетесь
с Политикой обработки персональных данных ×ЗАЯВКА СФОРМИРОВАНА УСПЕШНА
Числовой эквивалент стойкости к точечной коррозии (PREN)
Показатель RREN относится к справочным, он показывает склонность разных видов и марок нержавейки к появлению питтингов. Числовой эквивалент стойкости к точечной коррозии применяют как ориентир, но не как абсолютное руководство для предопределения коррозионной стойкости.
Обычно наиболее устойчивыми к точечному ржавлению оказываются молибден, хром и азот в качестве добавок при легировании. Чем выше цифра RREN, тем более стойкой будет сталь к появлению питтингов. Вот справочная информация по RREN:
| 444 | 25 |
| 430 | 16 |
| 304 | 19 |
| 316 | 26 |
| 304LN | 21 |
| 904L | 36 |
| 316LN | 27,5 |
| SAF 2507 | 42 |
| Zeron 100 | 41 |
к содержанию ↑
Особенности проявления катодной коррозии для разных типов металлов и сплавов
На особенности протекания коррозии влияет тип сплавов и металлов, которые контактируют друг с другом.
Все особенности сочетаний указаны в таблице ниже.
|
Тип металла |
Сочетания |
Примечания |
|
Алюминий и оксидированные сплавы. |
Магний и его оксидированные сплавы, прошедший пассивацию кадмий, разные типы стали – как окрашенной, так и оцинкованной, фосфатированной. |
Допускается применение сочетаний с низким риском появления коррозии как в жестких, так и в средних условиях. |
|
Магний и разные виды сплавов |
Магний и сплавы, в том числе, при покрытии грунтом и лаком, анодированный алюминий и сплавы, сталь с хромовым покрытием, а также с нанесенным сверху цинком, кадмием, оловом и другими видами продукции. |
Допускается применение сочетаний с низким риском появления коррозии как в жестких, так и в средних условиях. |
|
Медь и разные виды сплавов |
Никель, олово, хром, золото, анодированный алюминий. Допускается применение припоя оловянно-свинцового типа. Допускается сочетание с разными вариантами сплавов анодированного алюминия, окрашенной или фосфатированной стали. |
Допускается применение сочетаний с низким риском появления коррозии как в жестких, так и в средних условиях. |
|
Ценные металлы -родий, серебро, палладий, золото |
Все перечисленные виды металлов отлично сочетаются друг с другом с низким риском появления контактной коррозии. Можно также использовать изделия с оловом, никелем, алюминием, хромом и различными вариантами сплавов. |
—- |
|
Цинк и сплавы |
Сочетаются с разными вариантами стали, в том числе, хромникелевой, фосфатированной, окрашенной. В процессе обработки можно использовать в качестве припоя олово, а также его сочетание со свинцом. Среди других допустимых сочетаний – никель, анодированный алюминий и разные типы сплавов. |
—- |
|
Олово и сплавы |
Среди допустимых сочетаний можно назвать никель, хром, олово, медь, припои из сплава свинца и олова. Сталь в контакте может быть покрытой цинковым слоем, окрашенной или анодированной, если планируется использование в контакте с морской водой. Можно также использовать такой вариант материала с золотом и серебром. |
—- |
|
Хром и никель |
Одни из наиболее сочетаемых с другими разновидностями сырья. Список допустимых для контакта металлов очень большой – от золота, меди и сплавов до хрома, никеля, меди, цинка, кадмия и других. |
—- |
|
Кадмий |
Может соприкасаться с хромом, прошедшим процесс пассивации оловом, цинком, никелем, кадмием, припоем из олова и свинца. Сталь может быть как хромникелевой, так и хромистой, а также с дополнительным полимерным покрытием. |
—- |
Меры предосторожности для недопущения развития контактной коррозии
Чтобы риск контактной коррозии металла снизился, нужно соблюдать 3 рекомендации. К ним относятся следующие:
- Будьте осторожны с покрытиями. Это актуально в том случае, если планируется использовать изделие в районах с тропическим климатом и рядом с морем. Дополнительное покрытие не стоит наносить на участки деталей, где планируется сварка внахлест, установка заклепок из других видов сырья. Причина заключается в особенностях поведения электролита, когда коррозия значительно усиливается.
- При проведении сварки и клепки деталей, покрытие нужно снимать. После того, как все работы проведены, сверху можно будет наносить полимерное покрытие для борьбы с негативным воздействием окружающей среды.
- Не стоит использовать гальваническое покрытие в том случае, если перед вами деталь из черных или цветных металлов, прошедшие через литьевые формы.
Чтобы не допустить появления коррозии, всегда нужно понимать, с какими металлами вы работаете, и как они сочетаются друг с другом. Чтобы уменьшить степень интенсивности разрушения металла, нужно как можно скорее удалить соприкасающиеся отрезки сырья друг от друга.
Когда деталь используется в агрессивных средах, можно предусмотреть специальные прокладки. Хорошо справляется с задачей использования в морской воде магний и большинство его сплавов, цинк, алюминий и другие.
В качестве изоляции между элементами могут выступать металлические или полимерные лакокрасочные покрытия. Хорошим решением станут свинцовые детали.
Где возникает коррозия
Коррозия может возникать в чистой воде, сверхчистой воде, паре, очищенной питьевой воде или неочищенной технической воде. На сегодняшний день выявлено пять процессов.
Контаминация железом
Соединение нержавеющей стали с углеродистой сталью приведет к вытяжке железа на поверхности, которые будут подвержены ржавчине при пуске в эксплуатацию. Приваривание временных крепежей из углеродистой стали к нержавеющей стали с последующей шлифовкой швов приводит к истиранию хромированного слоя, который будет корродировать при эксплуатации системы. Использование проволочных щеток из углеродистой стали или шлифовальных кругов, загрязненных углеродистой сталью, приведут к образованию ржавчины. Механизм образования ржавчины весьма прост:
ЖЕЛЕЗО + ВОДА + РЖАВЧИНА,
Читайте также: ГОСТ Р 56731-2015 Анкеры механические для крепления в бетоне. Методы испытаний
Лучшее средство предупреждения образования ржавчины диктуется здравым смыслом: всегда покрывать все поверхности из углеродистого железа деревом, пластмассой или картоном во избежание контакта с нержавеющей сталью; никогда не приваривать углеродистую сталь к нержавеющей стали; всегда использовать щетки из исключительно нержавеющей стали и шлифовальные круги «предназначенные исключительно для нержавеющей стали»; всегда производить химическую пассивацию азотной или лимонной кислотой перед вводом в эксплуатацию.
Ржавчина может вызвать изъязвление или точечное образование ржавчины на нержавеющей стали под воздействием окислителя, поэтому она должна быть удалена. Поэтому необходима пассивация, которая не только увеличивает коэффициент наличия хрома (по отношению к железу на поверхности), но и предотвращает любую контаминацию железом. Используются два основных технических регламента для чистки и пассивации: «ASTM A 380 «Стандартные условия чистки, 2 удаления накипи и пассивации частей, оборудования и систем из нержавеющей стали»» и «ASTM A 967 «Стандартные условия обработки химической пассивации частей из нержавеющей стали». Как обработанная, так и не обработанная вода могут приводить к ржавлению (даже умягченная вода). Причиной является содержание воды – в первую очередь, бикарбонаты железа. Умягчение не удаляет анионы, такие как карбонаты, бикарбонаты, сульфаты, хлориды и т.п., а только обеспечивает обмен с катионами, такими как кальций и магний с содой и калием. В отличие от карбоната железа, бикарбонат железа полностью растворим, но легко окисляется до карбоната железа. Карбонат железа нерастворим и имеет буро-коричневый цвет. Он растворяется в сильных кислотах.
Обработанная или питьевая (пригодная для питья) вода обычно очищается для удаления взвешенных твердых частиц, фильтруется для удаления мельчайших частиц и, уничтоженных хлором или диоксидом хлора, бактерий. Данный процесс имеет незначительные последствия или не имеет последствий для ионов бикарбоната постольку, поскольку он уравнивается низким содержанием углеродистого железа в трубопроводе и содержанием кислорода. При попадании воды во внутреннюю среду, такую как нержавеющая сталь или фарфор, бикарбонаты начинают окисляться:
2Fe(HCO3)2 + Ca(HCO3)2 + Cl ® 2Fe(OH)3_+ CaCl2 + 4CO2 2Fe(OH)3 ® Fe203 + H2
Окись железа Fe203 становится бурым, и, когда это происходит, это называется появлением красного железняка. Сварной шов начинает корродировать, в связи с бурыми отложениями, по причине образования коррозионных элементов под воздействием ржавчины и хлорида кальция. В необработанной воде происходит подобная реакция, за исключением присутствия хлора, и кислорода, растворенного в воде, являющегося активным реагентом.
6Fe(HCO3)2 O2®2Fe2(CO)3_+2Fe (OH)2 + 4H2O
Карбонат железа начинает присутствовать и гидроксид железа образовывает желеобразную субстанцию, которая выявляется как окислы железа. Присутствует незначительное отклонение цвета, т.к. гидроксид железа желтого цвета. В больших резервуарах наиболее бурые отложения обычно сверху и уменьшаются ко дну. Весьма обычно наблюдать относительно чистое состояние большого резервуара.
Чистая и высоко очищенная вода
Чистая и высоко очищенная вода обычно используется в отраслях промышленности, где результат недостаточной очищенности может иметь существенные последствия: в таких как производство фармацевтической продукции или полупроводников. В фармацевтике она называется ВДИ или вода для инъекций. Типичная обработка предусматривает фильтрацию, умягчение, катионообмен и ионообмен, обратный осмос, обработку ультрафиолетом и, при необходимости, ионизацию. Процесс дистилляции может использоваться в качестве окончательной очистки. В результате получаем воду с чрезвычайно низкой проводимостью.
Нержавеющая сталь типа 316L — обычный материал конструкции оборудования. Некоторые из этих комплексов остаются чистыми, но некоторые другие – ржавеют. Даже системы, которые прошли электрополировку, имеющие шероховатость поверхности менее 10 микродюймов (<10 m-in Ra)
могут корродировать. В работе с горячим высоко чистым паром такие системы могут становиться черными, иногда, — блестяще черными, иногда, — черными с эффектом порошкообразного покрытия. Мы получили отдельные участки нержавеющего трубопровода, пораженного ржавчиной, из многих различных систем подачи чистой воды и пара. Слои ржавчины были исследованы рентгеноскопией(XPS), энергораспыляющей спектроскопией (EDS) и растрово-электронной микроскопией (SEM). Растрово-электронная микроскопия позволила произвести визуальное исследование поверхности, энергораспыляющая спектроскопия позволила по очкам проанализировать аномалии поверхностей, а рентгеноскопия позволила произвести послойный анализ ржавчины и выявление особенностей молекулярного строения. Подробные отчеты исследований приводятся в (1,2). Данное исследование позволило классифицировать процесс образования ржавчины в чистой и высоко чистой воде и паре по классам I, II и III.
Ржавчина класса I
Ржавчина класса 1 появляется от внешних источников. Частицы ржавчины откладываются на поверхности нержавеющей стали, и, на ранней стадии отложения, могут быть легко удалены промыванием. Пассивационный слой нержавеющей стали под ржавчиной остается неизменным с первоначально установленной системы. Частицы ржавчины обычно имеют тот же состав, что и материал, от которого происходят эти частицы (конечно же, не частицы, происходящие от корродирующей нержавеющей стали). Концентрация ржавчины наибольшая у источника водоснабжения и снижается в отдалении от него. Цвет ржавчины может изменяться, в зависимости от расстояния от источника, от оранжевого до красно-рыжего и ярко-красного на определенных участках. Коррозия, определяемая растрово-электронной микроскопией (SEM) класса 1, проявляется в качестве отдельных частиц. Цвет обуславливается наличием различных оксидов железа и гидроксидов. Оранжевый окисел является низшей степенью гидроксида железа, который образуется, если присутствуют одновременно кислород и вода:
2FeO+4H2O ®2Fe(OH) + 3H2
2Fe(OH) ® Fe2O3 + H2O.
Внешняя ржавчина может возникать от многих источников. Наиболее вероятны части из углеродистого железа, такие как стяжные шпильки, гайки, болты, струбцины и т.п. Чем больше источник, тем больше ржавчины может образоваться.
Насосы под наибольшим подозрением в системе очистки. Наиболее очевидными причинами ржавления, вызванными насосами, являются: изъязвление и эрозия, вызванные неравномерным вращением всасывающего колеса (крыльчатки). Изъязвление обычно вызвано неправильной подачей воды в насос, неправильным подбором насоса или излишним дросселированием при перекачивании. Пузырьки воздуха воздействуют на рабочие поверхности насоса и приводят к резкому воздействию, вызывающему ударную волну, удаляющую малые частицы нержавеющей стали. При освобождении частицы в водяном потоке она скрепляется со трубопроводом из нержавеющей стали посредством электростатического притяжения. Так как поверхность частицы не пассивирована, она незамедлительно начинает окисляться и ржавеет.
Читайте также: Металлические балки перекрытия размеры
Другим возможным процессом является эрозия крыльчатки. Любой материал имеет критическую величину вращения, сверх которой эрозия увеличивается (3). Для низколегированного сплава нержавеющей стали такая величина вращения составляет около 100 футов в секунду. Степень эрозии изменяется в зависимости от температуры. Нержавеющая сталь типа 304 имеет постоянную степень эрозии до температуры 300оС, а затем она стремительно возрастает. Не имеется специальных данных для воды высокой очистки для различных сплавов.
Металлургические свойства крыльчатки, как представляется, влияют на степень удаления металла водой. При кристаллизации нержавеющей стали 18-8 происходит две металлургические фазы: аустенита и дельта-феррита. Дельта-ферритовое образование зависит от состава сплава и, если он составляет менее 8%, оно может легко растворяться под воздействием нагрева. Отлитые лопасти насоса обычно имеют большее содержание дельта-феррита, так как во время отливки добавляется больше кремния для обеспечения текучести стали при литье. Это означает, что тепловое воздействие не приведет к растворению всего дельта-феррита. Причина, по которой дельта-феррит приносит больше проблем, состоит в том, что он подвержен большей эрозии, нежели аустенит и содержит больше железа.
Ржавчина класса II
Данный класс ржавчины возникает при присутствии хлоридов или других галогенидов. Это коррозия образующаяся и формирующаяся на поверхности нержавеющей стали в местах нарушения пассивирующего слоя. Данный тип ржавчины является неотъемлемой частью данной поверхности. Он наиболее часто появляется на непассивированных или механически полированных поверхностях и может свидетельствовать о точечной коррозии. Нержавеющая сталь под этими оспинами обычно очень потертая и может быть изъязвлена. При анализе состава этой ржавчины обычно обнаруживается присутствие хлоридов или других галогенидов. Ржавчину нельзя удалить иным механическим воздействием, нежели шлифовкой и полировкой, но чаще всего используется вытравливание кислотой. Лимонная кислота является хорошим чистящим средством пассивирует нержавеющую сталь, но при присутствии хлоридов поверхность будет вновь ржаветь.
Ржавчина класса II образуется в результате реакции из двух стадий: первая представлет собой растворение пассивационного слоя оксида хрома, а вторая состоит в окислении железа в материале:
Cr2O3 + 10Cl-+ 2H2O ® 2CrCl3 + 4 HClO 2Fe + 3ClO- ® Fe2O3 + 3Cl-
Данная реакция самоподдерживающаяся посредством взаимодействия хлора с хромом для образования гипохлористой кислоты в качестве побочного продукта, а гипохлористая кислота окисляет железо и образует еще больше хлорида.
Увеличение содержания молибдена в нержавеющей стали увеличивает ее стойкость к воздействию хлорида. Подобным образом, замена железа в нержавеющей стали никелем улучшает ее стойкость к коррозии. Прогрессия сплавов с увеличивающейся стойкостью к воздействию хлорида: тип 304L (наименьшая), тип 316L, тип 317L, тип 304LМ, Сплав 625, Сплавы С-276 и С 22 (наивысшая). При любом контакте нержавеющей стали с хлорангидридом возникает опасность образования ржавчины. Жесткость рН >7 имеет обеспечивает меньшую возможность образования ржавчины, нежели жесткость рН < 7. Даже кратковременное воздействие хлорангидрида может стать отправной стадией ржавления, в особенности, если поверхность нержавеющей стали шероховатая. Механически полированные поверхности хуже, нежели электрополированные поверхности, так как при полировальных операциях остаются микроскопические изъязвления. Электрополировка удаляет эти изъязвления и производит пассивирующий слой с более высоким соотношением Cr: Fe. Изъязвления образуют элементы коррозии, где могут концентрироваться растворы хлорангидрида и продолжать реагировать, даже если система в целом оснащена промывкой с высокой жесткостью воды. Использование сильнодействующих ПАВ в растворе промывки будет способствовать удалению хлорида.
Ржавчина класса III
Данная ржавчина черная, а не бурая и образуется в присутствии пара высокой температуры. При первоначальном образовании она синяя, а затем становится черной, поскольку она нарастает до предельной толщины, предупреждающей дальнейшее проникание кислорода. Она может обнаруживаться в паровых системах высокой чистоты, работающих при высоких температурах. На электрополированных поверхностях нержавеющей стали такая ржавчина блестяще черная, а на непассивированных механически полированных поверхностях она может быть матово черной. Ржавчина данного класса на электрополированной поверхности, образует октаэдрические кристаллы, полностью покрывающие поверхность. Анализ с использованием рентгеновской фотоэлектронной спектроскопии показывает, что данный слой является полуторной окисью железа, обычно именуемой магнитным железняком. Он не удалется обычной чисткой, но может быть удален химическими средствами или шлифованием. Если ржавчина является блестяще черной, то ее можно оставить, так как она достаточно стабильна. Матовое покрытие слоем ржавчины может быть удалено и может потребовать чистки. После химической чистки, обычно с использованием горячей щавелевой кислоты, поверхность должна быть химически пассивирована. При последующем пуске системы в эксплуатацию она вновь может почернеть, но, хотелось бы надеяться, без образования матового ржавого покрытия.
Данный тип ржавчины является продуктом реакции пара при высокой температуре с железом в нержавеющей стали, которая приводит к образованию магнитного железняка. Реакция происходит в два этапа:
3Fe0 + 4H2O ® FeO + Fe2)3 + 4H2 FeO + Fe2O3 ® Fe3O4
Часть оксида железа может замещаться оксидом никеля, но полуторная окись железа будет определять цвет покрытия.
Способы предохранения нержавейки от МКК
Очистить от ржавчины поверхность порой бывает сложно, особенно при глубоком проникновении дефекта. Разработан ряд методов против межкристаллитной коррозии, вот основные из них:
- Отжиг (стабилизирование). Ферритные стали обрабатывают высокими температурами (+750…+900 градусов), за счет чего концентрация хрома на поверхности повышается, при этом распределение элемента становится более равномерным.
- Уменьшение содержания углерода. Если концентрация вещества будет менее 0,03%, то металл станет практически не подверженным межкристаллитной коррозии.
- Закалка в воде. Этот метод применим для аустенитной стали, он помогает карбидам хрома перейти в более подходящую форму и сконцентрироваться на границах зерен металла.
Чтобы убрать у нержавейки склонность к МКК, в нее вводят и новые добавки: титан, тантал, ниобий, но это приводит к серьезному удорожанию материала. Их количество должно быть в 5-10 раз больше, чем норма углерода, и тогда металл будет не подверженным ржавлению.
к содержанию ↑
Коррозия и поверхностная обработка нержавеющей стали
Удаление коррозии можно произвести химическим способом – использовать специальные преобразователи ржавчины. Также поверхность изделий из нержавейки разрешается обрабатывать путем фрезерования, зачистки, шлифовки, полировки. Выбор конкретной методики зависит от предпочтений специалиста и ряда иных условий.
Подбор способа профилактической обработки металла будет обусловлен начальной коррозионной стойкостью конкретной марки стали. На шероховатых поверхностях чаще формируются элементы точечной коррозии, а на гладких пятна ржавчины появляются редко. Марки 304, 316 при использовании в условиях морской воды быстро ржавеют, их нужно защищать более тщательно.

к содержанию ↑